Las pruebas moleculares nos permiten identificar la presencia de material genético en una muestra clínica. En la actualidad, la prueba de Reacción en cadena de la Polimerasa con Transcriptasa Reversa en Tiempo Real (RT-PCR por sus siglas en inglés) es el estándar de oro para la detección del virus SARS-CoV-2, debido a su alta sensibilidad y especificidad (CDC, 2020). Esta prueba permite la transcripción del material genético del patógeno, de ARN a ADN, para posteriormente identificar secuencias específicas y únicas del virus que permitan su identificación de manera altamente específica.
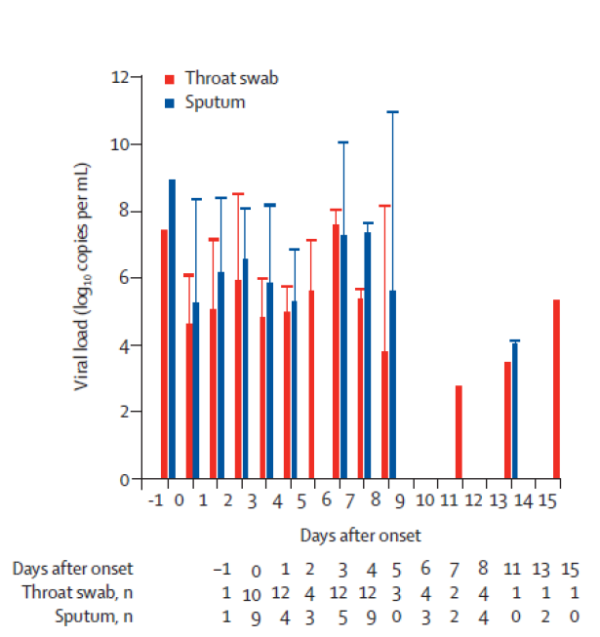
Figura 1. Detección de la carga viral del patógeno SARS-CoV-2 en muestras de hisopado faríngeo (color rojo) y esputo (color azul) en una muestra de 80 en diferentes estadíos de la enfermedad (Pan et al., 2020).
Sin embargo, como todo ensayo de laboratorio, los resultados de las pruebas moleculares deben de evaluarse de la mano con la clínica del paciente. El momento adecuado para tomar una muestra para la prueba RT-PCR es cuando el paciente presenta síntomas de la enfermedad. Se han realizado estudios analizando la carga viral de SARS-Cov-2, con respecto a los días de aparición de los síntomas. En una población de 80 pacientes diagnosticados con COVID-19, Pan et al. (2020) encuentran que la excreción del virus es irregular entre los pacientes muestreados, y la carga viral del patógeno (cantidad de material genético detectado) tiende a descender de manera importante a partir del día 9 de la aparición de los síntomas (Fig. 1). En este grafico también se muestra un paciente que fue muestreado un día antes del inicio de los síntomas, presenta una carga viral significativa. Este es un indicio importante de que los pacientes asintomáticos pueden tener una carga viral importante, por lo cual podrían ser potenciales dispersores del virus SARS-CoV-2.
Respuesta inmune ante el virus
La respuesta de anticuerpos nos puede brindar información relevante con respecto a la infección de SARS-CoV-2. Cuando en el organismo ingresan cuerpos extraños, como virus y bacterias, el organismo desarrolla una compleja respuesta inmune; dentro de este ataque coordinado, los linfocitos B producen anticuerpos o inmunoglobulinas que le permiten identificar y neutralizar de manera específica a los patógenos.
Existen 5 isotipos de anticuerpos en el organismo. Para el diagnóstico de enfermedades infecciosas, se utilizan las inmunoglobulinas G (IgG) y M (IgM) con mayor frecuencia, y con menor frecuencia la IgA. De manera clásica, se habla que la presencia de IgM en un paciente me indica que la enfermedad puede estar aún en su fase aguda, y que la presencia de IgG indica que el paciente ya superó la enfermedad. Diversas publicaciones indican que la respuesta inmune en pacientes de COVID-19 sigue este patrón, pero es necesario indagar más antes de llegar a una respuesta concluyente. Aún no se ha podido determinar durante cuánto tiempo se mantienen detectables las inmunoglobulinas anti SARS-CoV-2 en el organismo, pero ya se tiene una noción de cuándo estos marcadores empiezan a aparecer.
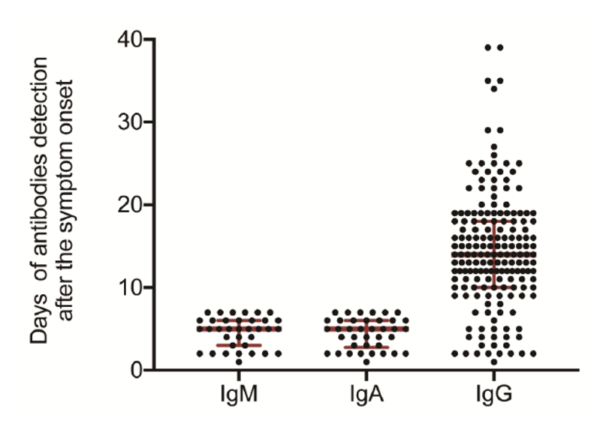
Figura 2. Respuesta de anticuerpos en pacientes de COVID-19 que presentaron sintomatología en los 7 días anteriores a la toma de la muestra. En el eje X se muestra los diferentes tipos de inmunoglobulinas (IgM, IgA e IgG), y en el eje Y los días en que detectaron los anticuerpos, posterior a la aparición de los síntomas (Guo et al., 2020).
El grupo de trabajo de Guo et al. (2020) realizó un estudio para entender la respuesta inmune mediada por anticuerpos en una población de 82 pacientes confirmados con COVID-19, y 58 pacientes sospechosos de portar la enfermedad. Los resultados obtenidos son interesantes, ya que nos muestran que los pacientes empiezan a mostrar anticuerpos detectables en promedio el día 5 posterior a la aparición de los síntomas, en el caso de las inmunoglobulinas IgM e IgA. En el caso de la IgG, el promedio de detección es en el día 14 a partir de la aparición de los síntomas (Fig. 2).
El grupo de investigación de Guo et. al (2020) también ha reportado que el diagnostico de COVID-19 incrementa de manera significativa cuando se aplica una estrategia en la que se implementen tanto detección de ácidos nucleicos como de anticuerpos: en una población de 140 pacientes con sintomatología asociada a COVID-19, nexo epidemiológico con pacientes previamente diagnosticados y radiografías de tórax altamente sugestivas de un cuadro producido por SARS-CoV-2, únicamente el 51% de los pacientes muestra un resultado positivo para RT-PCR. Sin embargo, se observa si se utiliza la prueba de anticuerpos IgM de manera conjunta, el índice de positividad en esta población aumenta a un 98.6% (Fig. 3(a)).
Anteriormente habíamos mencionado que la positividad de la prueba molecular comienza a descender de manera importante en pacientes con COVID-19, a partir del día 9 de aparición de los síntomas. Si la detección de anticuerpos contra SARS-CoV-2 empieza a ser positiva después del día 5 de aparición de los síntomas, se muestra que la utilización de ambas pruebas (RT-PCR y anticuerpos) es una estrategia más robusta para abordar el diagnóstico de la enfermedad.
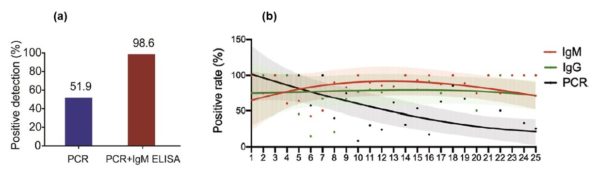
Figura 3. Diagnóstico de COVID-19 basado en la respuesta de anticuerpos. (a) Positividad de detección de casos de COVID 19 utilizando la prueba molecular (PCR), con respecto a una estrategia diagnóstica de utilización de pruebas moleculares y detección de anticuerpos. (b) Curva de mejor ajuste de la positividad de detección de la enfermedad COVID-19 utilizando pruebas moleculares (PCR) y detección de anticuerpos (IgM e IgG) mediante la técnica ELISA.
Por lo tanto, las pruebas de detección de anticuerpos o pruebas serológicas (debido a que utilizan como muestra suero sanguíneo) son un complemento interesante a las pruebas moleculares en el diagnóstico de COVID. En la Fig. 3(b) observamos que la positividad de la prueba molecular se mantiene mayor al 90% durante los primeros tres días a partir de la aparición de los síntomas, declina a un 80% en el día 6 de síntomas, y es menor al 50% después del día 14. Las pruebas serológicas tienen un comportamiento opuesto, teniendo una positividad mayor que la prueba molecular después del día 5 de aparición de los síntomas. La utilización de ambas pruebas brinda resultados más robustos y aumenta la sensibilidad del diagnóstico.
¿Cuál es el momento adecuado para aplicar una prueba diagnóstica específica?
La publicación realizada por el grupo de Sethuraman et al. (2020) resume de manera excepcional los hallazgos encontrados, con respecto a la variación temporal de la efectividad de las diferentes técnicas de detección de COVID-19 (Fig. 4). Antes de aplicar una prueba de detección a un paciente sospechoso, se debe tener claro el periodo de la enfermedad en la cual se encuentra el paciente. En los primeros días de la aparición de los síntomas, e incluso una semana antes, es decir, cuando el paciente aún no presenta síntomas, se han reportado cargas virales importantes en las muestras clínicas de los pacientes de COVID-19 bajo estudio. Estas cargas suelen descender rápidamente en el tiempo. Posterior a una semana de la aparición de los síntomas, empieza a elevarse el título de anticuerpos, que puede mantenerse detectable por semanas.
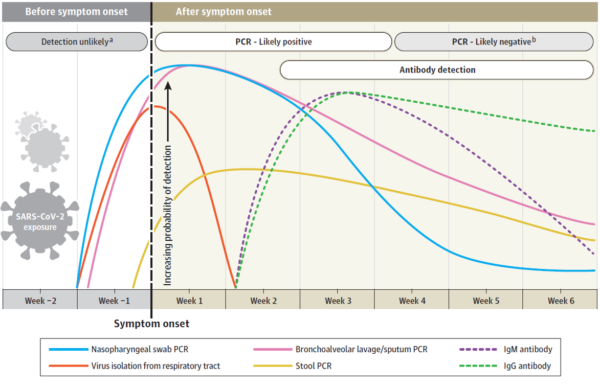
Figura 4. Variación temporal de la efectividad de las pruebas de diagnóstico de la infección de SARS-CoV-2, con base a la aparición de los síntomas.
Las pruebas serológicas tienen un papel primordial en estudios epidemiológicos, en los que se intenta dilucidar nodos de transmisión, buscando pacientes que pudieran haber resuelto la infección. En estos casos, la RT-PCR tiene una utilidad limitada debido a que su sensibilidad se restringe a casos agudos. El testeo serológico es especialmente útil en pacientes sospechosos de COVID-19, pero que ya se consideran recuperados, así como en pacientes asintomáticos o con sintomatología intermedia.
El monitoreo serológico es una herramienta importante para dilucidar la dinámica de la transmisión del virus, inmunidad poblacional y diseñar políticas de salud pública acordes al escenario actual (Yong et al., 2020). Así mismo, la prueba serológica para determinación de anticuerpos SARS-CoV-2 vendrá a complementar el diagnóstico de la infección, especialmente en pacientes con sintomatología relacionada a COVID-19 y cuyos resultados en la prueba RT-PCR sean negativos, para el testeo y monitoreo de personal esencial que pueda estar expuesto al virus (trabajadores de salud, policías, entre otros), para la elección de donadores de plasma convaleciente, y para dilucidar la respuesta inmunitaria respecto a las vacunas contra el virus SARS-CoV-2.
De esta manera, la implementación de un algoritmo diagnóstico en el cual se evalúe la presencia de anticuerpos IgG e IgM anti SARS-Cov-2, junto con la prueba RT-PCR puede ser una estrategia de detección más precisa y sensible, en el escenario de la actual pandemia.
Papel de las pruebas serológicas ante la aplicación de las vacunas
En Alemania se realizó un estudio clínico (Muller et.al. 2021), con la intención de dilucidar la respuesta inmune de anticuerpos posterior a la vacunación con el medicamento BioNTech/Pfizer. Se reclutó una población de 176 personas, clasificadas como jóvenes (menores de 60 años) y mayores (mayores a 80 años). El promedio de edad en el grupo de jóvenes fue de 42.2 años, en tanto en el grupo de mayores fue de 87.9 años. A todos los participantes se les tomó una muestra de sangre 17-19 días posterior a la primera dosis de la vacuna, y 17 días posterior a la segunda dosis.
Posterior a la primer dosis de la vacuna, el 93% de la población de jóvenes muestran anticuerpos IgG contra el virus SARS-CoV-2. El porcentaje de positividad de anticuerpos se eleva a un 100%, 17 días después de la segunda dosis. Sin embargo, el escenario es diferente en el grupo de personas mayores. Después de la aplicación de la primera dosis, únicamente el 24% de esta población mostraba anticuerpos IgG. El porcentaje de positividad de IgG aumentó a un 89.4% después de la segunda dosis (Fig. 5).
De manera adicional, se analizó la presencia de anticuerpos neutralizantes en la población estudiada, mediante la técnica de neutralización por reducción de placa (PRNT). En el grupo de jóvenes, únicamente el 16.1% de las personas mostraron anticuerpos neutralizantes ante el virus posterior a la primer dosis; sin embargo, este porcentaje aumentó al 97.8% luego de la segunda dosis. En el caso del grupo de mayores, únicamente el 1.2% desarrollo anticuerpos neutralizantes luego de primera dosis, el cual aumentó a un 68.7% posterior a la segunda dosis.
La disminución en la respuesta inmunitaria en el grupo de adultos mayores puede deberse a la inmunosenescencia, debido al decline de su respuesta inmune humoral y celular relacionado a la vejez (Muller et.al. 2021).
Este tipo de estudios generan discusiones sobre la necesidad de realizar testeos de anticuerpos en las poblaciones vacunadas antes de asumir inmunidad contra el virus SARS-CoV-2, especialmente en los adultos mayores y otros grupos de riesgo. Sin embargo, a la fecha no se ha dilucidado el protocolo a seguir.
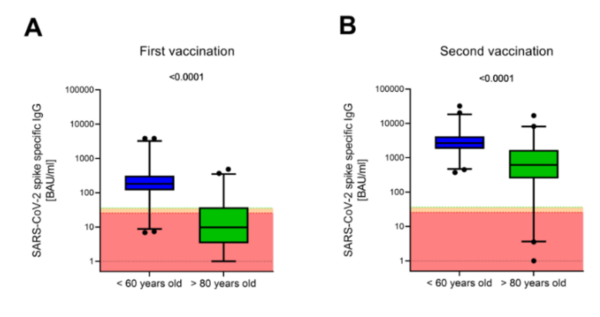
Figura 5. Título de anticuerpos específicos contra el Spike del virus SARS-CoV-2, en una población de personas jóvenes (menores de 60 años) y mayores (mayores a 80 años), a los que se le aplicó la vacuna BioNTech/Pfizer contra el virus SARS-CoV-2. Las cajas mostradas en los gráficos indican el 50% intermedio de los datos, la línea interna de los cuadros señala el promedio del grupo, y los bigotes delimitan los valores encontrados entre el 2.5% y 97.5% de los datos. La línea celeste indica el rango de cut-off de la prueba, y la zona rosada el rango de no reactividad del ensayo. A) Medición de anticuerpos anti-Spike 17-19 días posterior a la primer dosis de la vacuna. B) Medición de anticuerpos anti-Spike 17 días posterior a la aplicación de la segunda dosis de la vacuna.
Pruebas de Antígeno
Según el documento “LS-SS-012. Lineamientos generales para el uso de pruebas de antígeno para diagnóstico de COVID-19”, las pruebas de antígeno con hisopado nasofaríngeo podrán aplicarse en centros de salud de la Caja Costarricense del Seguro Social en pacientes sospechosos de COVID-19, que se encuentren entre el día 1 y 5 de aparición de los síntomas. Un resultado positivo será confirmatorio, en tanto los resultados negativos deben enviarse a la red de laboratorios de la CCSS para ser confirmados.
En el caso de los laboratorios privados, estos podrán aplicar las pruebas a personas que presenten tiquete aéreo para viajar fuera de Costa Rica. Los resultados positivos serán confirmatorios de COVID-19 y deben ser reportados ante el Ministerio de Salud. Los resultados negativos no descartan infección activa, y debe utilizarse únicamente como un trámite administrativo para viajar fuera del país.
Referencias bibliográficas
- Center for Disease Control and Prevention. Interim Guidance for Rapid Antigen Testing for SARS-CoV-2. https://www.cdc.gov/coronavirus/2019-ncov/lab/resources/antigen-tests-guidelines.html. Actualizado el 16 de agosto, 2020.
- Guo et al. Profiling Early Humoral Response to Diagnose Novel Coronavirus Disease (COVID-19). Clin Infect Dis. Publicado el 21 marzo 2020.
- Ministerio de Salud. LS-SS-012. Lineamientos generales para el uso de pruebas de antígeno para diagnóstico de COVID-19, versión 3. Publicado el 2 de febrero 2021.
- Müller et al. (Mar 5, 2021). Age-Dependent Immune Response to the BioNtech-Pfizer BNT162b2 COVID-19 Vaccination. Publicado el 5 de marzo en https://www.medrxiv.org/content/10.1101/2021.03.03.21251066v1.
- Pan et al. Viral load of SARS-CoV-2 in clinical samples. Lancet Infect Dis. Publicado el 24 de febrero, 2020.
- Sethuraman, et al. Interpreting Diagnostic Tests for SARS-CoV-2. JAMA. Publicado el 6 mayo 2020.
- Yong et al. Connecting clusters of COVID-19: an epidemiological and serological investigation. Lancet Infect Dis (20): 809–15. Publicado el 21 abril 2020.